从许可到备案 我国药品、医疗器械互联网信息服务管理迈入新阶段

自2024年1月20日起,我国对药品和医疗器械互联网信息服务的管理迎来了重大制度调整。根据国家相关部门发布的最新规定,此前实行的“药品、医疗器械互联网信息服务资格证”审批制度正式改为备案制度。这一变化标志着行业监管思路从严格准入的事前审批,转向加强事中事后监管的新模式,旨在进一步优化营商环境,激发市场活力,同时保障公众用药用械安全。
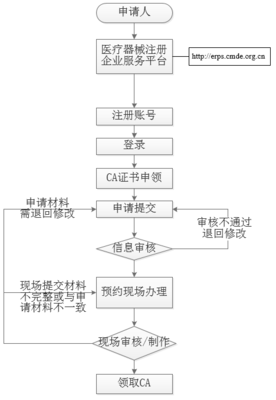
此次调整的核心在于简化流程,降低门槛。过去,企业从事药品、医疗器械互联网信息服务,需要向省级药品监督管理部门申请并取得相应的《互联网药品信息服务资格证书》或《互联网医疗器械信息服务资格证书》。审批流程相对复杂,时间周期较长。改为备案制后,符合条件的企业只需按照规定提交备案材料,完成备案手续即可开展相关服务,大大缩短了准入时间,为企业,特别是中小企业和创新型企业,提供了更便捷的准入通道。
从“许可”到“备案”,绝不意味着监管的放松。相反,这体现了“放管结合、优化服务”的监管理念。备案制度实施后,监管部门的职责重点将从事前审批转移到对信息服务提供者行为的持续监督和检查上。相关部门将建立健全以信用为基础的新型监管机制,通过加强日常监测、飞行检查、数据追溯等手段,确保网络信息服务的真实、准确、合规。对于在备案中提供虚假信息,或者在经营过程中发布违法违规信息、销售假冒伪劣产品等行为,监管部门将依法予以严厉打击,并纳入失信惩戒体系。这要求企业必须更加自律,切实承担起主体责任。
这一政策变革对行业将产生深远影响。对于广大消费者而言,合法合规的药品、医疗器械信息服务将更加丰富和便捷,获取健康信息的渠道得以拓宽。但同时也需提高警惕,增强辨识能力,选择在备案平台获取信息和服务。对于行业企业而言,既是机遇也是挑战。机遇在于市场准入更加便利,有利于业务创新和模式拓展;挑战则在于必须持续强化内部管理,确保线上信息的专业性、科学性和合法性,在更加开放透明的市场环境中接受全方位的监督。
总而言之,药品、医疗器械互联网信息服务管理改为备案制,是我国深化“放管服”改革、促进数字经济与健康产业融合发展的重要举措。它简化了行政程序,释放了市场潜能,并通过强化事中事后监管筑牢了安全底线。随着配套细则的完善和监管技术的进步,一个更加规范、高效、安全的药品医疗器械网络信息服务环境值得期待,最终将更好地服务于公众健康福祉和产业高质量发展。
如若转载,请注明出处:http://www.shuangdilegou.com/product/86.html
更新时间:2026-06-03 03:07:03